熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
摘要
背景:焦亡屬于一種新型炎癥性程序性細胞死亡途徑,子宮內膜癌的可能預后與終末蛋白 GSDMD 相關。氫氣對癌癥發揮雙重作用,通過促進腫瘤細胞死亡和保護正常細胞,這可能啟動了 GSDMD 通路介導的焦亡。
方法:我們進行了免疫組織化學染色和蛋白質印跡分析,以觀察 NLRP3、caspase-1 和 GSDMD 在人類和異種移植小鼠子宮內膜癌組織及細胞系中的表達。我們研究了氫氣處理是否可以通過細胞內和線粒體來源促進子宮內膜癌細胞中 ROS 的積累。使用 GSDMD shRNA 慢病毒轉染子宮內膜癌細胞以研究 GSDMD 蛋白在焦亡中的功能。使用碘化丙啶(PI)染色、TUNEL 檢測、測量乳酸脫氫酶(LDH)釋放和 IL-1β ELISA 來分析氫氣補充培養基或正常培養基之間的焦亡情況。我們在體內建立了人類子宮內膜腫瘤異種移植小鼠模型,以觀察氫氣補充的抗腫瘤效果。
結果:通過 IHC 和蛋白質印跡,我們觀察到在人子宮內膜癌和細胞系中 NLRP3、caspase-1 和 GSDMD 的過表達。氫氣預處理上調了 ROS 和焦亡相關蛋白的表達,并增加了 PI 陽性和 TUNEL 陽性細胞的數量,以及 LDH 和 IL-1β 的釋放;然而,GSDMD 敲低減少了它們的釋放。我們進一步證明,給小鼠補充氫氣足以產生抗腫瘤效果,抑制異種移植子宮內膜癌的體積和重量,因為飲用富氫水的小鼠顯示出降低的發光強度。HRW 組中的腫瘤組織切片呈現出 NLRP3、caspase-1 和 GSDMD 的中等至強陽性表達。氫氣通過焦亡途徑減弱了異種移植小鼠模型中的腫瘤體積和重量。
結論:這項研究擴展了我們最初關于氫氣在焦亡中刺激 NLRP3 炎癥小體/GSDMD 激活能力的分析,并揭示了在子宮內膜癌臨床管理中改善抗腫瘤效果的可能機制。
背景
子宮內膜癌是最常見的婦科癌癥。據美國癌癥協會估計,2019 年將有 61,880 例新的子宮內膜癌病例,12,160 名女性將死于子宮內膜癌。目前,對于無生育需求患者的治療仍以手術為基礎,而那些具有高危因素的患者還需要通過增加活性氧(ROS)介導的應激和激活細胞凋亡來殺死癌細胞的放療或化療。盡管可能發生與癌癥相關的凋亡誘導缺陷,但也可能出現“癌基因成癮”現象并導致治療失敗。因此,正在研究其他形式的細胞死亡以改善子宮內膜癌的預后。由于子宮內膜癌患者存在代謝綜合征引起的氧化應激升高和全身炎癥狀態,我們假設炎癥通路與子宮內膜癌的雌激素代謝方面同樣重要,并且炎癥介導的細胞死亡通路的激活可能有助于消除腫瘤細胞。
焦亡是一種炎癥性程序性細胞死亡途徑。它被稱為“pyroptosis”,因為“Pyro”源于希臘語“火”,等同于 caspase-1 和 IL-1β 的發熱和炎癥。“Ptosis”(“p”不發音)源自希臘語“falling”,意為其他形式的細胞死亡。焦亡現象最早在感染鼠傷寒沙門氏菌菌株的巨噬細胞中觀察到。隨后的細胞質腫脹、裂解和空泡化、膜孔形成、DNA 斷裂、染色質凝聚以及炎癥小體介導的 caspase-1 激活,以及促炎細胞因子 IL-1β 和 IL-18 的過量產生,導致細胞內容物釋放到周圍的微環境中,從而警示并招募鄰近細胞到達感染部位。
最近的研究結果表明,核苷酸結合域(NOD)樣受體(NLR)家族成員 pyrin 結構域包含蛋白 3(NLRP3)可以激活炎癥小體并觸發焦亡。功能性 NLRP3 炎癥小體的關鍵成分是 NLRP3、銜接蛋白凋亡相關斑點樣蛋白 ASC(一個 caspase 募集結構域,CARD)和促炎性 caspase-1。ROS/腫瘤壞死因子(TNF-α)/核因子-κB(NF-κB)信號傳導可以隨后誘導 NLRP3 激活。在這種細胞應激下,NLRP3 發生寡聚化并呈現聚集的 pyrin 結構域(PYD)用于與 ASC 的 PYD 結構域相互作用。ASC 的 CARD 然后與 pro-caspase-1 的 CARD 相互作用,從而實現 caspase-1 的激活。Caspase-1 僅參與焦亡而不介導凋亡,但 caspase-1 表現出兩個重要作用:(1)切割掉一個稱為 gasdermin D(GSDMD)的 53 kDa 蛋白的抑制性 C 末端結構域,并釋放 GSDMD 的成孔 N 末端結構域,然后自組裝在質膜上形成孔道;以及(2)將促炎細胞因子 IL-1β 和 IL-18 的前體轉化為其活性形式,最終介導炎癥過程為焦亡。人類 gasdermin 基因家族成員 GSDMD 最近被確定為焦亡的關鍵執行者,并且 GSDMD 蛋白需要激活劑,如 LPS 和尼日利亞菌素,來啟動死亡信號;然而,這些激活劑僅限于實驗室使用,并且已被證明難以在臨床上轉化。因此,找到可以轉化為臨床應用的安全有效的激活劑非常重要。
雙原子氫(H2)對癌癥發揮抑制腫瘤細胞生長和保護正常健康細胞的雙重作用。生物膜對 H2 相當通透,因為它們可以擴散到細胞質、線粒體和細胞核中,這與它們的分布特性有關。
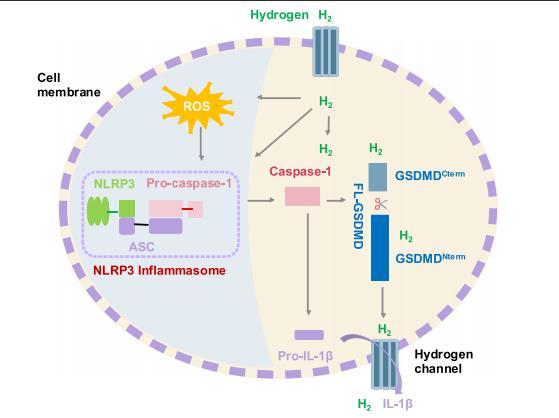
圖1:氫氣在細胞和組織中的分布示意圖。氫氣 (H2) 可自由擴散穿過生物膜進入細胞質、線粒體和細胞核。相比之下,大多數親水性抗氧化劑無法穿透生物膜。ROS:活性氧。
相比之下,大多數親水性抗氧化劑不能穿透生物膜,而是留在膜表面。在體溫下,H2 可用作惰性氣體,或溶解于水或生理鹽水中,在大氣壓下濃度高達 0.8 mM(1.6 ppm),以產生富氫水或富氫鹽水,或用于產生產氫納米材料。在過去 10 年中,H2 已被用于治療癌癥和代謝性疾病或糾正各種器官的缺血再灌注損傷,利用其高生物安全性。關于癌癥,氫氣可以以劑量和時間依賴的方式抑制宮頸癌、乳腺癌、皮膚黑色素瘤、卵巢癌、肺癌、結腸癌、胸腺淋巴瘤、艾氏腹水腫瘤細胞、口腔鱗狀細胞癌和纖維肉瘤細胞的細胞活性、增殖、侵襲和遷移;促進細胞凋亡;減少腫瘤體積和重量;并抑制異種移植小鼠的腫瘤生長,從而延長荷瘤小鼠的存活時間。H2 還能減輕接受放療和化療患者的腎毒性。因此,氫氣療法受到越來越多的關注,現在被認為是一種有前途的治療方法。
我們實驗室的初步數據表明,氫氣在子宮內膜癌細胞中誘導了 TNF/NF-κB 和凋亡途徑。然而,目前尚無關于 H2 是否也能激活焦亡,或者如果發生化療或放療引起的凋亡抵抗,它如何在子宮內膜癌中發揮作用的現有報告。目前也不清楚 H2 是否在子宮內膜癌中抑制腫瘤生長,以及其機制是什么。